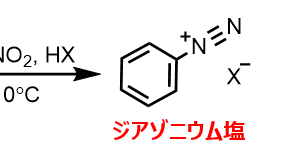
ジアゾニウム塩の調製
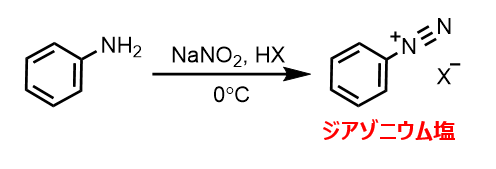
ジアゾニウム塩は、種々の置換基を導入できるSandmeyer(ザンドマイヤー)反応やアゾ化合物の合成で用いる、非常に有用な化合物です。
これを知っていれば、反応経路を問われる問題で経路の一つとなることも少なくないので、求電子剤や反応条件について理解しておきましょう!
反応機構
アニリンの窒素上の非共有電子対に対する求電子剤として反応するのはニトロソニウムイオン(+NO)です。
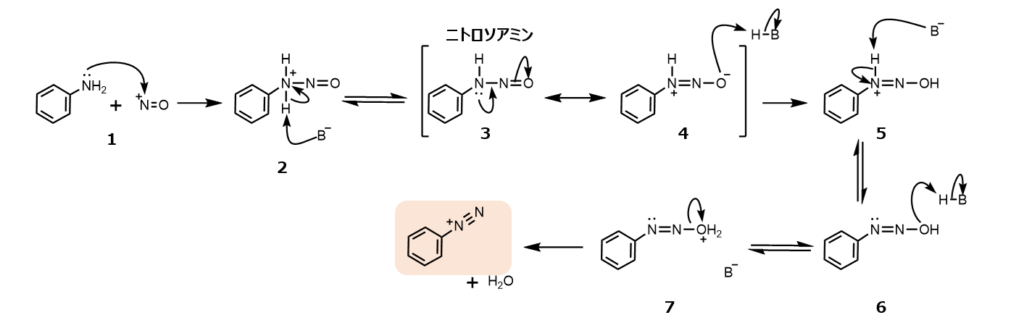
- アニリン窒素原子上の非共有電子対にニトロソニウムイオンが付加する
- 塩基によるプロトン引き抜きにより、ニトロソアミンが生じる
- 共鳴により、酸素原子上に電荷が移動
- 酸素がプロトン化される
- 塩基によるプロトン引き抜き
- ヒドロキシ基がプロトン化される
- 水として脱離して、ジアゾニウムイオン(塩)が生成する
長い反応機構に見えますが、+NOが付加して、水が抜けるという流れをおさえておけば、すんなり頭に入ってきます。
ニトロソニウムイオン(+NO)源
ジアゾニウムイオン調製には、ニトロソニウムイオン(+NO)が必要です。
芳香環のニトロ化の際に必要なニトロニウムイオン(+NO2)と混同しないようにしましょう。
ニトロソニウムイオンの発生には、亜硝酸ナトリウムNaNO2、ハロゲン化水素HXを用います。
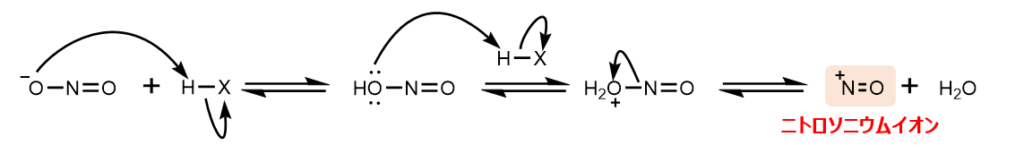
ニトロ化で必要なニトロニウムイオン、スルホン化で必要なスルホニウムイオンと同様に、酸からプロトンを受け取って、H2Oが脱離することにより求電子剤が発生します。
反応について
低温で行う理由
ジアゾニウムイオンは、熱や光により安定な窒素とカチオン(次いでフェノールとなる)に分解してしまいます。
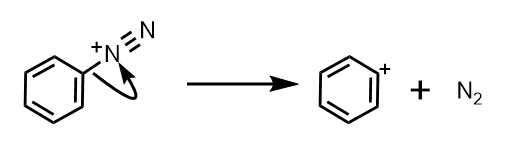
窒素は不活性ガスとして用いられているように、安定なのはご存知だと思います。したがって、一度活性化エネルギーの山を乗り越えてしまえば元には戻れません。
室温程度の熱には、活性化エネルギー(エネルギー障壁)を乗り越えさせるのに十分なエネルギーがあるため、氷水などを用いて低温で行うのです。
このように、ジアゾニウムイオンは不安定なイオンであるため保存には向いていません。
一部の芳香族ジアゾニウム塩は保存できるようですが、基本的にジアゾニウムイオンが必要な反応を行う直前に調製します。
ジアゾニウム塩の使い道【Sandmeyer反応・Schiemann反応・ジアゾカップリング】
調製したジアゾニウム塩はSandmeyer反応やSchiemann反応、ジアゾカップリングに用います。
Sandmeyer反応
アレーンジアゾニウムイオンと銅(Ⅰ)塩の反応により、ジアゾ基がCuXのXと置換する反応をSandmeyer反応と呼びます。


以下のように、ジアゾニウム塩とハロゲン化銅(Ⅰ)の反応によりハロゲンが、シアン化銅(Ⅰ)との反応によりシアノ基が導入できます。
ヨウ素化については、カリウム塩(KI)で行うことができます。フッ素化は後述。
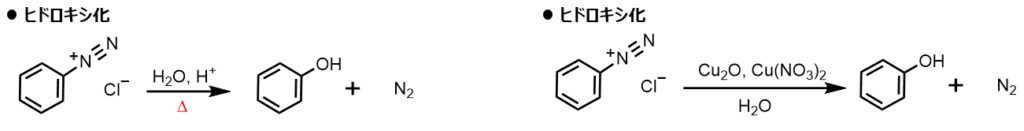
その他にも、ジアゾニウム塩の酸性水溶液を加熱することでヒドロキシ基が置換してフェノールが生成します。
また、酸化銅(Ⅰ)/硝酸銅(Ⅱ)の水溶液を加えることにより、収率よくヒドロキシ化する方法もあります。
Schiemann反応
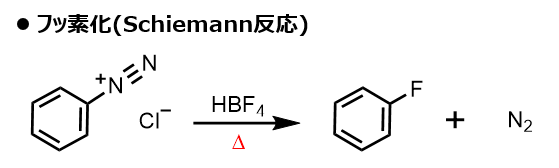
ジアゾニウム塩に四フッ化ホウ素(HBF4)を加えて加熱することで、フッ素化物を得る反応はSchiemann(シーマン)反応と呼ばれます。
ジアゾカップリング
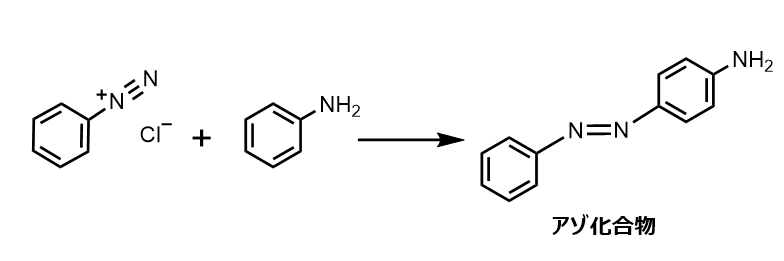
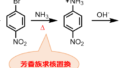
ジアゾニウムイオンが求電子剤として芳香族求電子置換反応し、アゾ結合(-N=N-)を形成する反応をジアゾカップリングと呼びます。
この際、反応する求核剤は強く活性化されたベンゼン環(-NH2, -NRH, -NR2, -OH)である必要があります。活性化/不活性化置換基については活性化/不活性化基置換基と配向性をご覧ください。
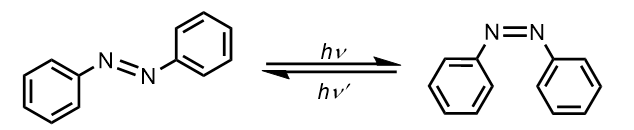
ちなみにですが、アゾ化合物には光によりtrans-cisの異性化が起こるという面白い性質があります。
まとめ
- アニリンに亜硝酸ナトリウムNaNO2、ハロゲン化水素HXを加えるとジアゾニウム塩が生成する
- NaNO2, HXはニトロソニウムイオン+NOを発生させ、これが求電子剤となる
- 低温で反応を行うのは、ジアゾニウムイオンの分解を防ぐため
- ジアゾニウムイオンを原料としてSandmeyer反応、Schiemann反応、ジアゾカップリングが行える
- ハロゲン、シアノ基、ヒドロキシ基を導入したかったら、
アニリン→ジアゾニウム塩→Sandmeyer, Schiemannも一つの方法

コメント