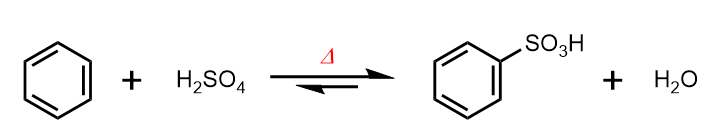
芳香族環は濃硫酸とともに加熱することで、スルホン化することができます。
スルホン化はハロゲン化、ニトロ化、Friedel-Crafts反応と同様に芳香族求電子置換反応により進行します。
したがって、求電子剤が必要になるわけですが、スルホン化における求電子剤はスルホニウムイオンとなります。
反応機構
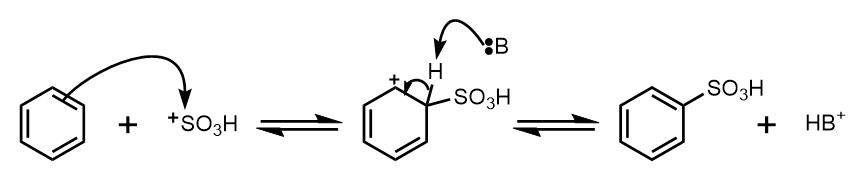
- 電子豊富な芳香環に、求電子剤(スルホニウムイオン+SO3H)が付加する
- 系中の水などの塩基がプロトンを引き抜いて、芳香環を再生する
スルホニウムイオン源
ニトロ化に必要な求電子剤(ニトロソニウムイオン)は、硝酸と硫酸の混酸により発生させていました。
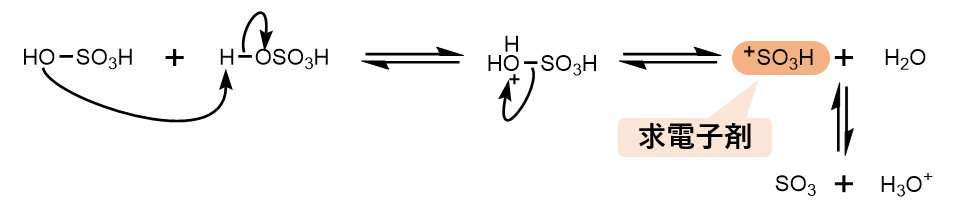
スルホン化の場合、硫酸による硫酸のプロトン引き抜きがわずかに起こるため、ここから水が脱離することでスルホニウムイオン(+SO3H)が発生します。
また、スルホニウムイオンは水を介して三硫化硫黄(SO3)と平衡にあります。
したがって、濃硫酸に三硫化硫黄を吸収させた発煙硫酸を用いることでスルホニウムイオンを効率的に発生させることができます。
反応について
脱スルホン化
スルホン化は可逆反応であるため、スルホン化した芳香環に酸を加えると脱スルホン化することができます。
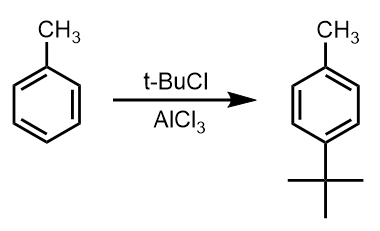
例えば、トルエンのオルト位だけにtert-ブチル基を導入したい場合を考えてみましょう。
アルキル基の導入をFriedel-Crafts反応で行うとします。
まず、メチル基(アルキル基)は電子供与性基であり、オルト/パラ配向性となります。
Friedel-Crafts反応における求電子剤はカルボカチオン、今回の場合かさ高いtert-ブチルカチオンなのでオルト位よりも立体障害のないパラ位の方に付加しようとします。
これを防ぐために、スルホン化によりパラ位を塞いじゃいます!
スルホン酸基はかさ高いので、tert-ブチル基同様パラ位に優先的に付加します。
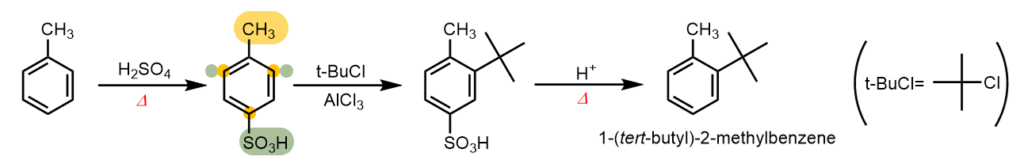
アルキル基はオルト/パラ配向性、SO3H基はメタ配向性であるため、次の求電子置換反応により導入される基は図のように2つの配向性が一致するとこに付加します。
よって、2つ目の化合物に対してFriedel-Crafts反応を行うことで、tert-ブチル基をメチル基のオルト位だけに導入することができますね。
ここで、酸を加えて加熱することにより脱スルホン化を行うことで、目的の化合物を得ることができました!
まとめ
- 芳香環は、濃硫酸との加熱でSO3H基を付加できる(スルホン化)
- 機構は芳香族求電子置換反応であり、必要な求電子剤はスルホニウムイオン(+SO3H)
濃硫酸に三硫化硫黄を吸収させた発煙硫酸では、求電子剤を効率的に得られる。 - 可逆反応なので、酸/加熱でSO3H基を取り除ける!
これを利用して、簡単な保護ができる

コメント