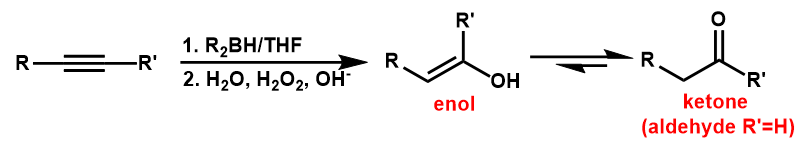
アルキンをケトンやアルデヒドに変換する方法として、ヒドロホウ素化-酸化があります。
アルケンの場合は、ヒドロホウ素化-酸化は逆マルコフニコフ的にアルコールに変換する方法でした。
アルキンの場合、アルケンと同様に考えると、生成するのは不安定なエノールなので、ケト-エノール互変異性化によりケトン/アルデヒドへと変換されます。
試験で逆合成の問題が出されたとき、アルキン→ケトンの変換が中々出てこないと思いますので、アルキンの水付加と合わせてあるアルキンからどのようなケトンが合成できるのか理解しておきましょう。
反応機構
反応を大まかに分けると、
①アルキンのヒドロホウ素化
②酸化反応
③ケト‐エノール互変異性化
の3つで構成されます。
・アルキンのヒドロホウ素化
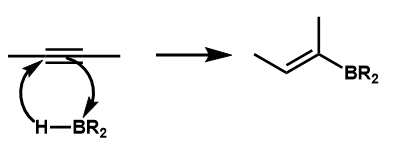
- ホウ素が求電子剤として働き、アルキンのπ電子を受け取り結合形成すると同時に、ヒドリドイオン(BH3のH-)が求核剤として、ホウ素と結合してないほうの炭素に結合する
また、R2BH/THFのTHF(テトラヒドロフラン)の役割についてはこちらをご覧ください。
・酸化反応
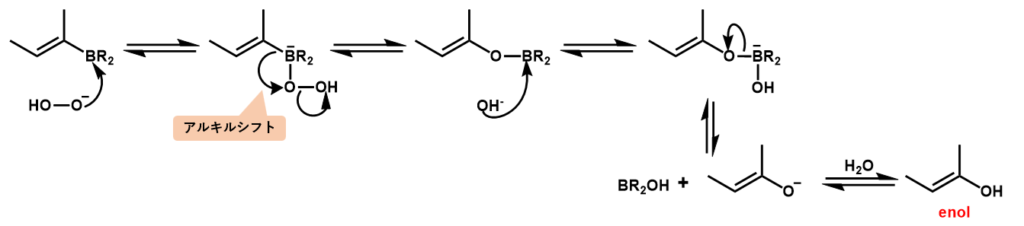
- 過酸化水素イオン(–OOH)が求核剤として、ホウ素に電子供与
- ホウ素上の負電荷を解消するため、アルキル基が酸素上に転位して、水酸化物イオンが脱離
- 水酸化物イオンが求核剤として、ホウ素に電子供与
- エノラートとして脱離することで、ホウ素上の負電荷解消
- エノラートが水からプロトンを受け取ってエノールを生成
※エノールのOHからプロトンが脱離してO-となっている陰イオンをエノラートと言います。
・ケト‐エノール互変異性化
ヒドロホウ素化-酸化により得られた化合物は不安定なエノールなので、より安定なケトンもしくはアルデヒドに変換されます。
アルキンの水付加では、酸により互変異性化が触媒されていましたが、
ヒドロホウ素化-酸化の場合、塩基により触媒されます。
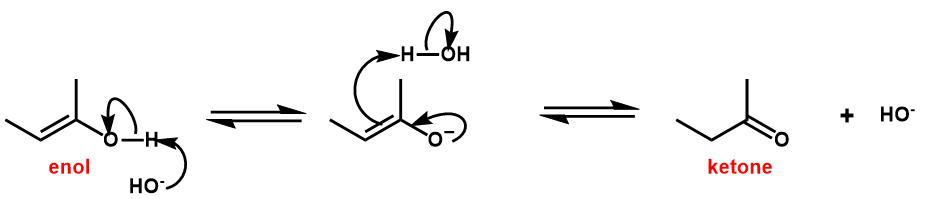
- 塩基によるエノールのプロトン引き抜きが起こる
- 炭素‐炭素間のπ結合が切れてプロトンと結合する代わりに、炭素‐酸素間のπ結合が生成する
エノール→ケトへの変換をみると、
酸触媒の場合、C=C↔C=Oの変換が起こってからプロトン引き抜きですが、
塩基触媒の場合、プロトン引き抜きが起こってからC=C↔C=Oの変換という順番になります。
(もちろん、ケト→エノールから見れば逆の順番となります。)
酸触媒なら正電荷を経由する経路、塩基触媒の場合負電荷を経由する経路をとるということを知っていればすぐに分かります。
この例では、生成物はケトンでした。アルデヒドとなるのはどんな時でしょうか。↓
反応について
末端アルキンの場合
三重結合が主鎖の末端にある末端アルキンでは、生成物はアルデヒドとなります。
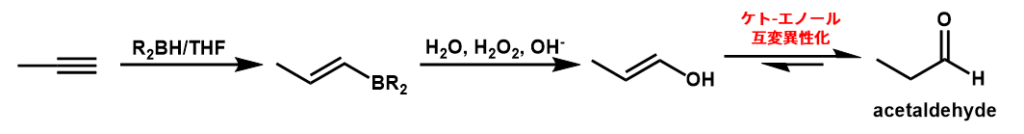
水付加の場合では、末端アルキンに水を付加しようとすると内部の炭素にOHがつくため、生成物は常にケトンでした。
ヒドロホウ素化-酸化の場合、BR2基が末端アルキンの外側の炭素について、それがOHに変換されるのでケト型はアルデヒドとなります。
keto-enolのketoはketone(ケトン)だけでなくアルデヒドも含まれるので、注意して下さいね!
まとめ
- アルキンのヒドロホウ素化-酸化は大まかに3つに分けられて、
①ヒドロホウ素化(BH3/THF)
②酸化反応(H2O2/OH–/H2O)→エノールの生成
③ケト-エノール互変異性化
により、ケトン/アルデヒドが合成できる。 - 末端アルキンの場合、生成物はアルデヒドとなる。

コメント