アルケン+水→アルコール
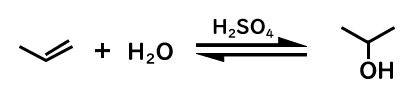
アルケンの二重結合部分は、電子豊富なため求核攻撃をすることができます。
アルケンが求核攻撃して、ハロゲン化水素が付加すると、ハロゲン化アルキルが生成します。
では、ハロゲン化水素と同じようにH2Oが反応すると、HとOHでアルコールが生成しそうですが、ただの水を加えただけでは、Hが付加してOH–が生じるというのは滅多に起こりません。
水の付加反応を進めるためには、触媒として酸が必要となります。
酸の働きは、H2Oをプロトン化してH3O+とすることです。それにより、Hが付加したときに、残りはH2Oとなります。
H3O+→H2Oの方が、H2O→OH–よりも容易なため、反応が進行するようになります。
OH–、H2OをそれぞれH2O、H3O+の脱離基とみると、OH–よりもH2Oの方が弱塩基なので、脱離しやすい、と考えるのがおすすめの考え方です。
塩基性と脱離のしやすさは、アシル化合物の反応と合わせて学んでおくとお得です。
反応機構
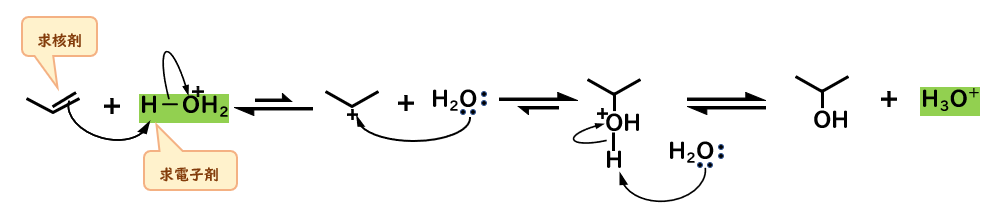
- アルケンがプロトンに対して求核攻撃して、カルボカチオンを生じる
このとき、プロトンが付加する炭素は、マルコフニコフ則に従う。 - H2Oの酸素の非共有電子対がカルボカチオンに対して求核攻撃して結合
- 水が塩基としてプロトンを引き抜き、アルコールの生成とともに触媒が再生
1段階目のプロトンの付加は、最も多く水素が結合している方の炭素に対して行われます。(Markovnikov則)
理由は簡単に、その方が安定なカルボカチオンを生じるからです。詳しく見ておきたい方はこちらで確認しておきましょう。決して暗記しようとしないでくださいね!
中には、

生成したアルコールの酸素が求核剤になって、カルボカチオンに攻撃してエーテルになりそうだけど?
という疑問を持つ方もいると思います。
確かに、アルコールが求核剤として働いてエーテルを生成することは可能です。
実際に反応している様子を思い浮かべてみましょう。
水和反応では普通、ほかの分子より水の方がたくさんあるので、溶液は水の濃度が高いはずです。
したがって、カルボカチオンが生成したアルコールに出会う確率よりも、水と出会う確率の方が圧倒的に高いため、エーテルはほとんど生成しません。
同様の理由で、HSO4–がカルボカチオンと反応することは滅多にありません。
反応について
カルボカチオンの転位
ハロゲン化水素の付加同様、反応途中でカルボカチオンを経由するため、カルボカチオンの転位を考える必要があります。
3,3-ジメチル-1-ブテンの反応をみてみましょう。
マルコフニコフ則に従ってC-1にプロトンが付加して、3,3-ジメチル-2-ブタノールが生成するでしょうか。

実際には、それは副生成物となります。
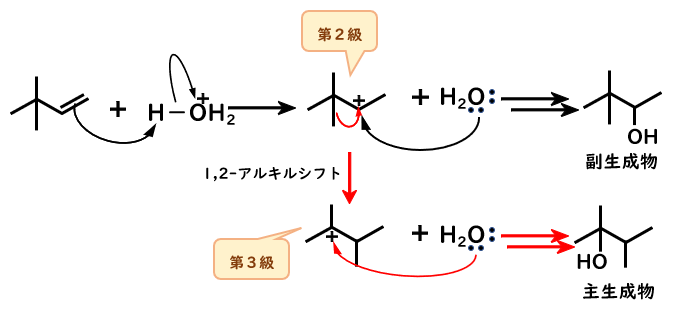
反応機構を見てみると、マルコフニコフ則に従い、第2級カルボカチオンが生成した後、
多くのカルボカチオンは、正電荷の隣の原子であるC-3についているメチル基が正電荷をもつ炭素に移動(シフト)して、C-3に正電荷が移ります。
したがって、主生成物は2,3-ジメチル-3-ブタノールとなります。
まとめ
- アルケンと水は酸触媒を加えることで反応し、アルコールを生成する。
- 反応の流れは、
「H3O+からのプロトン付加」→「カルボカチオンと水の結合」→「プロトン引き抜き」 - カルボカチオンは、マルコフニコフ則に従い安定なカルボカチオンを生じる
- カルボカチオンの転位を考えるのを忘れない




コメント