酸無水物→カルボン酸
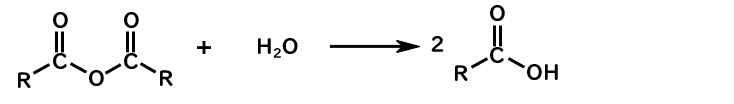
酸無水物→エステル
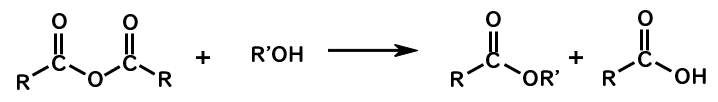
酸無水物→アミド
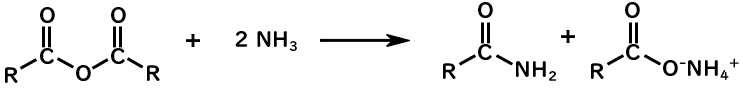
2つのカルボン酸から脱水した組成を持つ酸無水物は、カルボン酸のOH基がカルボキシラートイオンで置換されたアシル化合物です。
アシル化合物類を反応性順に並べると、酸無水物はハロゲン化アシルよりは低く、エステル/カルボン酸よりは高いです。
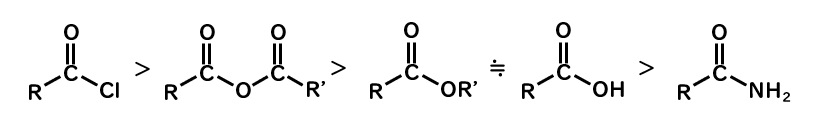
アシル化合物の反応性は、脱離基の塩基性の強さにより決まります。
また、アシル化合物の反応点はカルボニル炭素であり、
弱い塩基ほど電子を与える能力が低い(そして、脱離能高い)ので、カルボニル炭素の求電子性が高いです。
酸無水物の脱離基であるカルボキシラートイオンの塩基性は、Cl– < RCOO– < RO–,OH– *なので上の反応性順序になることが分かります。
*共役酸の酸の強さがHCl > RCOOH(カルボン酸) > ROH, H2Oであることから簡単に分かります。
(共役酸の酸性が強いほど、その塩基は弱い)
ちなみに、2分子の酢酸が脱水縮合した無水酢酸は、有用なアセチル化剤(アセチル基CH3CO-を導入できる)です。
鎮痛剤であるモルヒネに無水酢酸を混ぜて煮て、OH基をアセチル基に置換することで、薬物依存性の強いヘロインが合成できてしまいます。
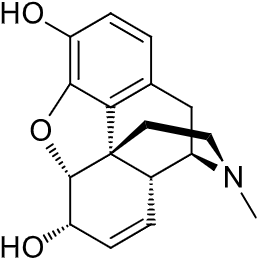
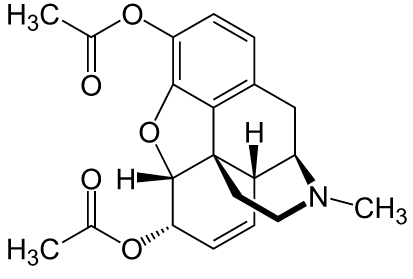
1)Wikipedia, https://ja.wikipedia.org/wiki/%E3%83%A2%E3%83%AB%E3%83%92%E3%83%8D, (2/19/22)
2)Wikipedia, https://ja.wikipedia.org/wiki/%E3%83%98%E3%83%AD%E3%82%A4%E3%83%B3, (2/19/22)
そのため、法律により、無水酢酸は麻薬原料として取引が規制されていたりします。
反応機構
無水酢酸が水と反応してカルボン酸を生成する反応を例にとって見てみます(せっかく脱水してあるのに戻すのは勿体ないと感じますが)
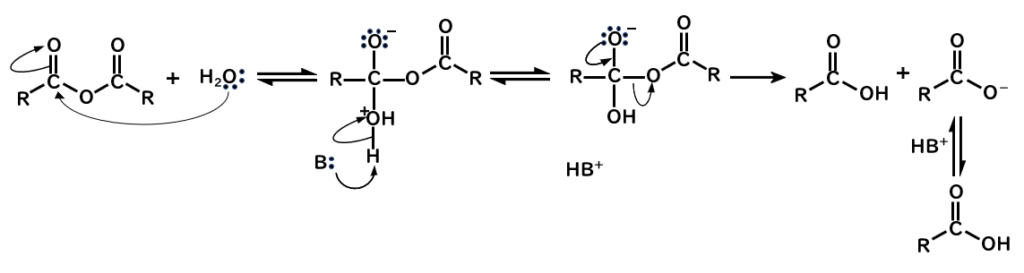
- 求核剤として水がカルボニル炭素に攻撃して、四面体中間体を生成
- 塩基がプロトンを引き抜く
- より弱い塩基の-OCORが脱離し、カルボン酸、カルボキシラートイオンが生成
(カルボキシラートイオンはカルボン酸と平衡をとる)
こうしてみると、塩化アシルの反応機構とほとんど一緒であることがわかると思います。
アルコールが反応するときは、求核剤の水をアルコールを置き換えるだけで、酸無水物→エステルとなります。
ただし、塩化アシル→アミドのときと同様に、酸無水物→アミドは少し注意が必要です↓
反応について
酸無水物→アミドはアミンが2当量必要
酸無水物にアミン、アンモニアが反応してアミドを生成するときには、2当量のアミン、アンモニアが必要となります。
1当量反応した時点では、アミドとカルボン酸が生成します。
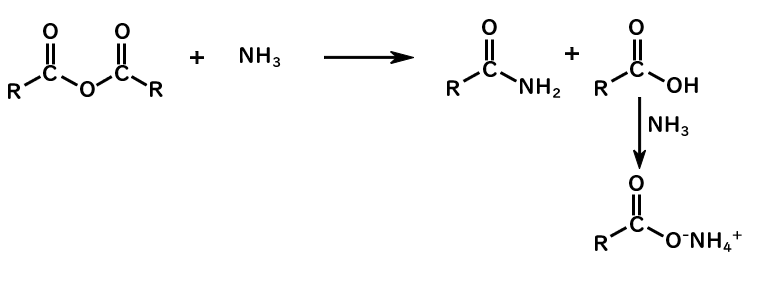
ここで、溶液には塩基性のアミン(アンモニア)が多く存在するので、発生したカルボン酸と即座に反応して塩となります。
つまり、1当量分は求核剤として、もう1当量分は塩基として必要になってくるわけです。
まとめ
- 酸無水物の反応性は、エステル/カルボン酸よりは高く、ハロゲン化アシルよりは低い
- 酸無水物 + アルコール → エステル + カルボン酸
酸無水物 + 水 → 2*カルボン酸
酸無水物 + 2*アミン →アミド +カルボン酸塩
であり、反応機構は塩化アシルの反応と同様 - アミンが2当量必要なのは、カルボン酸の中和のため



コメント